Реконструкция дефектов с применением аллогенных трансплантатов
Результаты реконструкции вертлужной впадины аллогенными трансплантатами в 447 случаях за 10 лет
К. Фризеке • К.Б. Отто
Реферат
Значение трансплантации гомологичных костей возрастает. Результаты операций по замене улучшились с того времени, когда был основан костный банк. Появилась возможность лечения обширных дефектов с помощью трансплантатов. Это произошло благодаря созданию распределительной системы и накопления необходимого опыта в центрах. Большое число подготовительных действий значительно уменьшает ожидание успеха. В настоящее время не имеется лучшей альтернативы. Вероятность приживления трансплантата составила 93% за восемь лет. Вероятность приживления вертлужной впадины составила, как определили по асептическому расширению вертлужной впадины в качестве критерия исключения, 86% за восемь лет.
При возрастающем числе операций протезирования бедренного сустава, хирурги будут всё чаще сталкиваться с патологией костного вещества в области вертлужной впадины. В ходе этого развития гомологичные реконструкции при замене вертлужной впадины приобретают всё большую важность (5, 6).
С 1976 по 1998 гг. в Эндо-клинике Гамбурга было проведено 17 300 асептических операций и дополнительно около 5 000 одномоментных операций при околопротезной инфекции; только за истёкший год выполнено 1 100 асептических и 250 септических замен.
С 1983 г. мы содержим костный банк. За это время мы отобрали 11 000 головок бедренной кости при первичных имплантациях. Из них 7 900 головок были трансплантированы, 2 900 пришлось – преимущественно по бактериологическим основаниям – исключить. В настоящее время в 55% операций полного эндопротезирования мы трансплантируем гомологичные кости, причём эта тенденция возрастает. Отсюда возникает необходимость, чтобы подобного рода центры повторных суставных операций, которые содержат костный банк, сохранялись и далее.
Материалы и методы
Все трансплантаты были получены от живых доноров. Это относится к головкам бедренной кости, которые были удалены во время первичной имплантации эндопротеза сустава. Их преимущества по сравнению с отбором из трупов заключаются, во-первых, в высоко стерильных условиях отбора, а во-вторых, в точном сборе анамнеза, который иногда становится причиной исключения донора. И то, и другое повышает безопасность реципиента.
Все прочие серологические и бактериологические исследования как донора, так и трансплантата проводятся стандартно, и затем все головки сохраняются при –70°.
Все трансплантаты, которые применяли в представленном исследовании, были глубоко заморожены без обработки сразу же после отбора. Из-за расширяющихся проблем передачи возбудителей заболеваний, головки бедренной кости стали стандартно инкубировать с прогревом согласно марбургской системе. При этом достигается внутренняя температура в трансплантате 80° по Цельсию. Настоящим исследованием охватываются все 447 последовательных замен вертлужной впадины с 1983 по 1985 гг., которые дополнительно содержали аллогенный трансплантат вертлужной впадины. Время наблюдения в этом ретроспективном исследовании составляет от восьми до двенадцати лет, а в среднем десять лет. 358 пациентов (ок. 80%) были женщины, 89 (ок. 20%) мужчины. Возраст пациентов варьировал от 24 до 89 лет и в среднем составил 61 год.
Основным диагнозом был коксартроз в 157 случаях (35%), диспластический коксартроз в 165 случаях (37%), ревматоидный артрит в 36 случаях (8%), посттравматический артроз в 31 случае (7%), постинфекционный артроз в 13 случаях (3%) и прочие диагнозы в 45 случаях (10%).
У 42% пациентов была операция по назначению, уже по меньшей мере третья операция, и множество предшествующих перенесённых операций вызвало повреждения мягких тканей и костей.
Типы дефектов в вертлужной впадине классифицировали по системе Нидера (3, 4). Система основана на том главном принципе, что каждое расширение происходит вслед за общим расширением ложа имплантата, и после этого вертлужная впадина имеет три различных возможности миграции. Она перемещается либо краниально, либо кранио-латерально, либо кранио-медиально. Этим обусловлены специфические утраты костной ткани в вертлужной впадине, затрагивающие те костные структуры, которые лежат по направлению миграции. Четыре различные формы повреждений соответствуют указанным типам классификации по Нидеру: расширенный тип (тип I), краниальный тип (тип II), диспластический тип (тип III) и протрузионный тип (тип IV). Последний дополнительно определяется тем, что ещё представлена костная медиальная граничная пластина (тип IVa), либо представлено открытое дно вертлужной впадины (тип IVb).
В литературе описано много различных схем для классификации потери костного вещества в области вертлужной впадины. Большинство из них относительно сложны, не согласованы и трудно применимы на практике. К тому же, эти схемы не дают указаний на вид проводимой реконструкции. В классификации по Нидеру дело обстоит иначе, и в этом её преимущество перед другими схемами. Во-первых, она проста и наглядна, с тем последствием, что её всегда возможно применить на практике. Во-вторых, из типа дефекта следует вид проводимой костной реконструкции. Поэтому для нас система Нидера оказалась очень полезной как во время операции, так и перед ней и после неё. Мы классифицировали случаи по типам: 76 случаев (17%) – тип I, 127 случаев (28%) – тип II, 87 случаев (20%) – тип III, 148 случаев (33%) – тип IVa, 9 случаев (2%) – тип IVb.
Результаты
В 75% случаев для реконструкции применяли костные блоки. При этом только малые несовпадения заполняли срезами губчатой кости. В 19% случаев применяли только срезы кости, и в 6% случаев реконструкция дефектов не определена.
К моменту исследования 11% пациентов уже умерли, а 12% были недоступны. По крайней мере, в рамках статистики выживания, многих из них всё же возможно оставить в нашем исследовании, поскольку в это время они находились под регулярным наблюдением. Данные 77% пациентов оценивали на основании рентгеновских снимков, а также клинических исследований и анкетного опроса. В среднем за десять лет в 371 случае (83,2%) не произошло повторного расширения вертлужной впадины, в 59 случаев (13%) развилось асептическое расширение, и в 17 случаях (3,8%) септическое расширение вертлужной впадины. Принимая во внимание большое число предшествующих операций, длительность операции и включение в учёт поздних инфекций за время срока службы в среднем десять лет, доля инфекций 3,8% приемлема и не отличается от доли при заменах без трансплантата.
Анализ 76 (16,8%) расширенных вертлужных впадин в сравнении с общим числом пациентов показывает статистическую значимость (p > 0,01) большего числа предшествующих операций в группе со вновь расширенными вертлужными впадинами. Это означает, что с увеличением количества предшествующих операций возрастает риск новой несостоятельности элемента вертлужной впадины. В отношении первичного диагноза, больше расширений оказалось связано с основными диагнозами диспластического коксартроза и ревматоидного артрита, хотя и без статистической значимости. Не обнаружено статистически значимого возрастания в связи с типом излеченного дефекта.
Все 76 (16,8%) расширенных вертлужных впадин были снова заменены. Во время этих повторных операций исследовали трансплантат. При этом в 48 случаях мы обнаружили резорбцию трансплантата, в том числе и во всех 17 случаях инфекции, а в 28 случаях – продолжающий там находиться in situ трансплантат. В этих случаях несостоятельность вертлужной впадины было невозможно приписать отказу трансплантата. Кроме того, интегрированный трансплантат послужил для нового усиленного укрепления вертлужной впадины.
Кривая выживания по Каплану-Мейеру показала вероятность выживания 93% для трансплантата после 8 лет. В отношении компонента вертлужной впадины в асептических случаях за то же время получилась вероятность выживания 86%, а для суммы всех расширений (септических и асептических) она составила 82%. Такие цифры – гораздо лучше, чем в более раннем исследовании, где – раньше основания костного банка – костные дефекты в вертлужной впадине заполняли цементом. Далее будет представлен обзор операций на основании примерных случаев.
Тип I: Типичная морфология при общем расширении вертлужной впадины показывает небольшую потерю окружающего костного вещества без перемещения вертлужной впадины. При замкнутом дефекте реконструкция методически проста, и выполняется с использованием среза губчатой кости с последующим цементированием имплантации вертлужной впадины. Возможно применение стандартных имплантатов для установки в положение первичной вертлужной впадины (рис. 1).
Тип II: В краниальном типе наблюдается типичная морфология с дефектом кости в области крыши вертлужной впадины. Выступ вертлужной впадины в полном порядке, а медиальная граничная пластина всегда сохраняется. Реконструкцию выполняют с использованием среза губчатой кости (раздробленного трансплантата), поскольку он показывает лучшие результаты в процессе приживления, чем крупные структурные блоки. Исходным условием является наличие закрытого дефекта (огороженного дефекта). Здесь тоже возможно применение малого стандартного имплантата для установки в первичную вертлужную впадину (рис. 2).
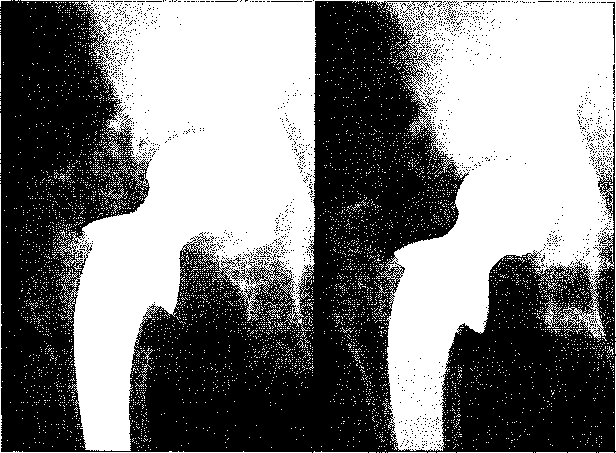
Рис. 1. Тип I: Общее расширение ложа вертлужной впадины. Предоперационный рентгеновский снимок, и результат через девять лет после реконструкции срезом губчатой кости.

Рис. 2. Тип II: Краниальный тип. Потеря вещества в крыше вертлужной впадины с сохранным выступом и лишь минимальным медиальным дефектом, и состояние через десять лет после реконструкции срезом губчатой кости.
Тип III: Диспластический тип, морфологически отличается от краниального типа тем, что потеря в крыше вертлужной впадины ограничена, тогда как весь выступ вертлужной впадины отсутствует. Дно вертлужной впадины не повреждено. Реконструкцию необходимо выполнять структурным трансплантатом, т. к. отсутствует окружающий структурный дефект. Возможна альтернатива с опорной чашкой. Фиксацию трансплантата кости мы проводили двумя параллельными винтами, которые, по возможности, должны лежать по направлению образованного тазобедренного сустава, во избежание перелома винтов (рис. 3).
Тип IV: Самый обширный дефект кости развивается в протрузионном типе. Морфологически, выступ вертлужной впадины всегда сохранен, потери в крыше вертлужной впадины незначительны, но при протрузии вертлужной впадины происходит потеря в области дна вертлужной впадины.
В закрытом типе (IVa), с сохранившейся костной граничной пластиной в медиальном направлении, выполняют реконструкцию со срезом губчатой кости.
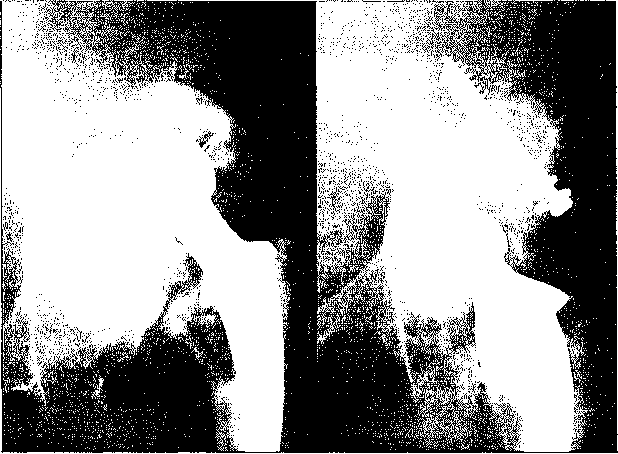
Рис. 3. Тип III: Диспластический тип. Потеря выступа вертлужной впадины после кранио-латерального смещения впадины, и вид через 12 лет после реконструкции структурным трансплантатом. Направление фиксирующего винта вдоль образованного бедренного сустава.
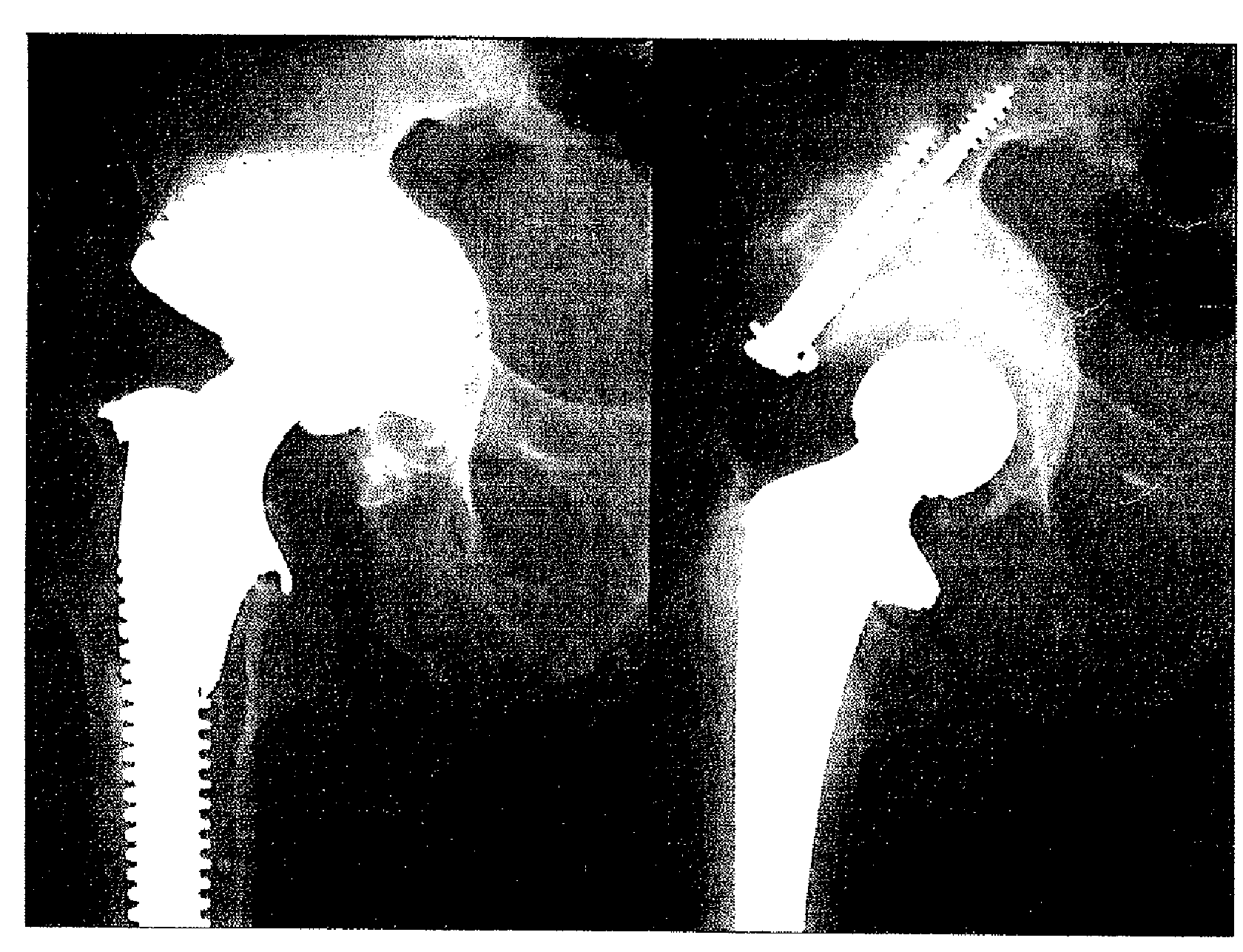
Рис. 4. Тип IVa: Закрытый протрузионный тип. Смещение вертлужной впадины без цемента в медиальном направлении, с ещё сохранившейся костной граничной пластиной, и состояние через 11 лет после реконструкции срезом губчатой кости в дне таза, с дополнительной структурной пластикой крыши с целью обеспечения имплантации стандартной впадины в первичную вертлужную впадину.
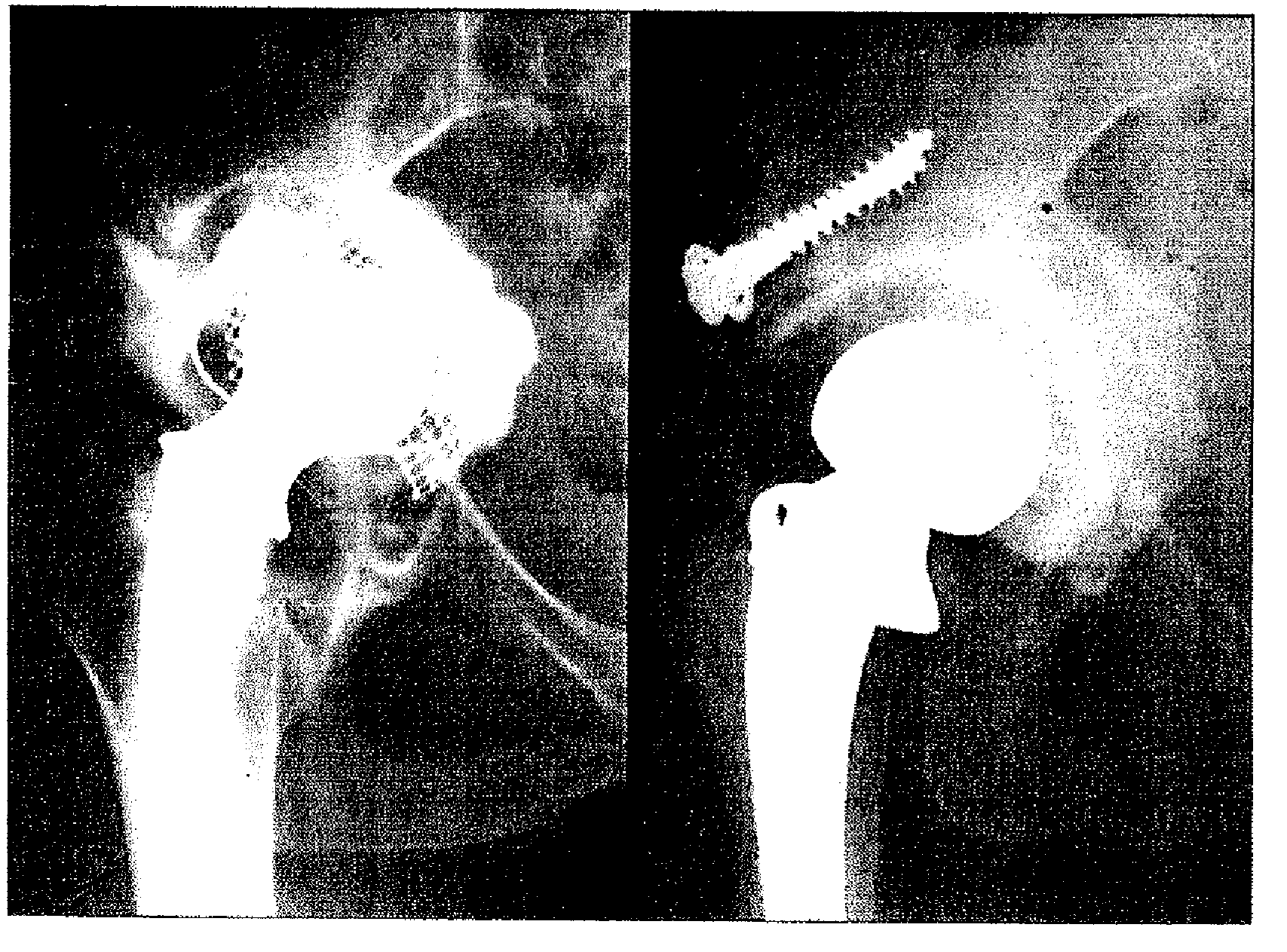
Рис. 5. Тип IVb: Открытый протрузионный тип. Предоперационное состояние с открытым дном таза после центрального смещения вертлужной впадины, и вид через 8 лет после установки структурного трансплантата в вертлужную впадину с дополнительной структурной пластикой крыши вертлужной впадины.
Применение структурных трансплантатов требуется только тогда, когда дополнительно представлен дефект в крыше вертлужной впадины (рис. 4). Вертлужную впадину следует имплантировать с достаточно сильной латерализацией, во избежание новой протрузии. Металлические опорные кольца и/ или чаши требуются не обязательно. Вместо стандартной вертлужной впадины возможно использование впадины с полиэтиленовым воротником.
В открытом протрузионном типе (IVb) с отсутствием дна вертлужной впадины невозможна реконструкция со срезом губчатой кости. Он представляет собой самый трудный для реконструкции дефект. В таких случаях необходимо вставлять структурный имплантат, чтобы перекрыть центральный дефект. Затем выравнивают несовпадения с помощью срезов губчатой кости (рис. 5). Имеет смысл применение дополнительных металлических конструкций, как например, пластин Кербула. По крайней мере, следует имплантировать полиэтиленовую впадину с воротником.
В случаях с нестабильным тазом возможность костной реконструкции вертлужной впадины зачастую уже невозможна. Как альтернатива, имеется в распоряжении имплантация вращательного седловидного протеза (1, 2). В этих случаях седловидный протез составляет конкуренцию замене крупных частей таза или трансплантации крупных костей от трупа. Все эти методы имеют высокий процент осложнений.
Литература
(1) Friesecke, C.: Results of saddle prosthesis (Endo-modell) in hip revision. In: Hip International 3, 170–171 (1999) [Результаты с седловидным протезом (модель Эндо) при повторной операции на тазобедренном суставе]
(2) Nieder, E., Friesecke, C., Plutat, J.: Ergebnisse von 73 Implantationen der Sattelprothese MK II ENDO-Modell in der Revisionsalloarthroplastik. In: Kerschbaumer, F., Nieder, E., Rehart, S. (Hrsg.): Die Hüftendoprothese in komplizierten Fällen. Thieme, Stuttgart, 179–195 (1995) [Результаты 73 имплантаций седловидного протеза модели MK II ENDO при повторной аллогенной пластике суставов]
(3) Nieder, E.: Revisionsalloarthroplastik des Hüftgelenkes. In: Bauer, R., Kerschbaumer, E., Poisel, S. (Hrsg.): Orthopädische Operationslehre Bd. 2/1. Becken und untere Extremität. Thieme, Stuttgart, 619–673 (1994) [Повторная аллогенная пластика тазобедренного сустава]
(4) Nieder, E.: Revision total hip arthroplasty. In: Bauer, R., Kerschbaumer, E., Poisel, S. (Hrsg.): Atlas of hip surgery. Thieme, Stuttgart, 217–332 (1996) [Повторная полная пластика тазобедренного сустава]
(5) Otto, K.B., Baars, G.W., Nieder, E.: Beckenknochendefekte in der Alloarthroplastik. In: Orthopäde 16, 226–276 (1987) [Дефекты тазовой кости в аллогенной пластике]
(6) Otto, K.B., Nieder, E., Klüber, D.: Major loss of acetabular bone stock at revision total hip arthroplasty. In: Czitrom, A.A., Winkler, H. (Hrsg.): Orthopaedic allograft surgery. Springer, Wien, 113–1176 (1996) [Обширная утрата кости в вертлужной впадине при повторной полной пластике тазобедренного сустава]
